Типы рн-метров, принцип их действия и технические характеристики
Содержание:
- Обзор косметики с рН, оптимальным для кожи
- Крем-гель для лица с розовой водой для сухой и чувствительной кожи, Garnier
- Очищающий гель «Абсолютная нежность» для сухой и чувствительной кожи, L’Oréal Paris
- Очищающая эмульсия Nutri:nectar, Shu Uemura
- Очищающая пенка для лица Biosource Self-Foaming Cleansing Water, Biotherm
- Очищающий тоник «Чистая кожа» против черных точек и жирного блеска, Garnier
- Тоник «Роскошь питания», L’Oréal Paris
- Увлажняющий лосьон для сухой и очень сухой кожи лица и тела, CeraVe
- Концентрат-активатор молодости двойного действия Advanced Génifique Sensitive, Lancôme
- Почему среда во влагалище кислая?
- Нормальные значения
- Приготовление раствора и калибровка
- рН в организме человека
- Измерение водородного показателя
- Самостоятельное определение pH
- Роль pH в химии и биологии.
- 2.Причины
- Показания
- Набор для калибровки Ph-метра
Обзор косметики с рН, оптимальным для кожи
Есть средства для чувствительной кожи с рН, далеким от нейтрального.
Крем-гель для лица с розовой водой для сухой и чувствительной кожи, Garnier
Особенность средства состоит в том, что его моющая и пенящаяся основа — кокобетаин, производное кокосового масла. Поэтому крем-гель мягко очищает кожу и обладает физиологическим рН. Подробнее о продукте
Екатерина Турубара
Медицинский эксперт Vichy
«Очищающие средства на базе омыляемых липидов масла карите или кокосового пригодны для всех типов кожи: от самой сухой и поврежденной до жирной и склонной к образованию комедонов».
Очищает кожу при помощи масел, не пересушивая. Даже стойкий макияж удаляется сразу. Успокаивает благодаря витамину В5 и экстракту лилии в составе. Подробнее о продукте
Очищающий гель «Абсолютная нежность» для сухой и чувствительной кожи, L’Oréal Paris
В основе — производные кокосового масла и масла карите. Экстракты розы и жасмина придают гелю успокаивающие свойства. Подробнее о продукте
Схема ухода за чувствительной кожей
Очищающая эмульсия Nutri:nectar, Shu Uemura
Масло-эмульсия подходит для умывания сухой кожи, очищает и насыщает ее антиоксидантами и жирными кислотами омега из ягод асаи и магнолии. Подробнее о продукте
Очищающая пенка для лица Biosource Self-Foaming Cleansing Water, Biotherm
Пенка не только очищает, но и ухаживает за чувствительной кожей, поскольку содержит экстракт термального планктона. Подробнее о продукте
Очищающий тоник «Чистая кожа» против черных точек и жирного блеска, Garnier
Как и у всех тоников, основная его задача — нормализация рН кожи. Продукт содержит салициловую кислоту и цинк, но не пересушивает кожу, склонную к жирности. Подробнее о продукте
Тоник для лица
Тоник «Роскошь питания», L’Oréal Paris
Тоник подойдет для любого типа кожи. Он содержит питательные масла розы и камелии (чая), а также витамин Е. Подробнее о продукте
Увлажняющий лосьон для сухой и очень сухой кожи лица и тела, CeraVe
Средство с легкой текстурой быстро впитывается и увлажняет кожу на 24 часа. Благодаря церамидам, которые являются составной частью кожных липидов, укрепляется гидролипидная мантия.
Концентрат-активатор молодости двойного действия Advanced Génifique Sensitive, Lancôme
Как известно, рН тесно связан с микрофлорой кожи. Так что пробиотики в составе концентрата тоже способствуют правильному рН-балансу. Подробнее о продукте
Почему среда во влагалище кислая?
Вещество, называемое влагалищным секретом, на самом деле вырабатывается не во влагалище. В этом органе отсутствуют железы, способные производить его. Жидкость, которая является основой так называемого секрета, проникает во влагалище из кровеносных сосудов в его слизистой оболочке. Этот процесс называется транссудация. Кислотность этой жидкости близка в нейтральной, как и pH крови. Также весомую часть секрета составляет слизь, выделяемая шейкой матки.
Почему же влагалищный секрет имеет кислую реакцию? Это связано с деятельностью лактобактерий, живущих в этом органе. Они вырабатывают молочную кислоту, которая при условии концентрации не менее 0,5% , помогает уничтожать инфекционных агентов, попадающих на слизистые оболочки влагалища.
За сутки во влагалище взрослой здоровой женщины производится примерно от 0,76 до 4,5 мл секрета. В нём обязательно обнаруживаются лактобатерии в больших количествах, объёмы другой микрофлоры в норме намного меньше.
Во время гинекологического обследования доктор обязательно обращает внимание на состав влагалищного секрета. В зависимости от соотношения его составляющих различают три степени чистоты влагалища:
- Первая. В секрете есть много лактобактерий и отсутствует патологическая микрофлора. Эпителиальные клетки и лейкоциты обнаруживаются в умеренных количествах.
- Вторая. В секрете присутствует большое количество лактобактерий и эпителиальных клеток, также есть небольшое количество лейкоцитов и представителей патологической микрофлоры.
- Третья. Лактобактерий (палочек Дедерлейна) в секрете мало, зато в избытке обнаруживаются лейкоциты и представители патологической микрофлоры.
- Четвёртая. Лактобактерии в секрете полностью отсутствуют, зато очень много патологических микроорганизмов. Эпителиальные клетки выделяются в умеренных количествах.
Естественно, что отсутствие лактобактерий, вырабатывающих молочную кислоту, изменит реакцию секрета. Поэтому предварительно диагностировать изменение чистоты влагалища можно при помощи теста на кислотность. Конечно, полную картину даёт только обследование у гинеколога, но посещать его очень часто не получится, а тест полоски pH всегда под рукой.
Нормальные значения
Показатель кислотности урины обусловлен следующими особенностями:
- возрастной категории пациента (у взрослых и детей);
- гендерной принадлежности (у женщин и мужчин);
- временем суток (утро и вечер);
- особенностями питания (преобладание в рационе белковых, растительных или молочных продуктов);
- наличием хронических заболеваний (эндокринной, мочевыделительной системы, желудочно-кишечного тракта).
У женщин на кислотно-щелочной баланс оказывает влияние беременность и кормление грудью. Нормальный уровень pH колеблется в интервале от 5 до 7 единиц. Согласно принятым лабораторным нормам, здоровой считается слабокислая реакция мочи. Оптимальным значением в данном случае является pH 6.
Детские показатели
У ребенка грудного возраста кислотность мочи зависит от особенностей питания (искусственные смеси или естественное вскармливание), а также от времени появления на свет относительно срока беременности (доношенный или недоношенный).
| Младенцы, родившиеся в срок | Недоношенные дети | Искусственники | Малыши на естественном вскармливании |
| от 5,4 до 5,9 ед. | от 4,8 до 5,4 ед. | от 5,4 до 6,9 ед. | от 5,6 до 6,0 ед. |
Нестабильный pH у новорожденного грудничка не вызывает опасений при условии, что нет генетических патологий и врожденных аномалий развития. Нормализация уровня происходит на 3–4 день. У детей и подростков до совершеннолетия норма pH мочи укладывается в границы от 6,5 до 7,5 единиц.
Уровень у взрослых мужчин и женщин
На показатель кислотности у взрослых мужчин влияет мышечная масса (ММ), у женщин – перинатальный период и лактация. При беременности допускается незначительное превышение референсных значений.
| Мужчины | Женщины | |||
| средняя ММ | высокая ММ | не беременные | беременные | кормящие |
| 6,3–6,5 | 6,5–7,2 | 6,0–6,5 | 5,0–8,0 | 6,5–6,8 |
Отклонения краткосрочного характера наблюдаются в ночное время и утренние часы (до завтрака). Уровень pH может снижаться до 5,2 ед. утром, и повышаться вечером до 7 ед. Такие «качели» опасности не представляют. Неизменное значение кислотности утром и вечером, не выходящее за пределы нормативных границ, к патологиям не относится. Если же в течение суток реакция остается стабильно кислой или стабильно щелочной, возникает необходимость в дополнительном обследовании.
Дополнительно
Закисление урины (ацидоз) фиксируется при показателях pH 5 и ниже. Мочевая кислота, соли фосфорной и щавелевой кислот взаимодействуют с жидкостями, у которых уровень кислотности имеет нормальные или чуть завышенные показатели. При снижении pH до 5 единиц и менее, они превращается в осадок.
Стабильно высокий уровень кислотности провоцирует образование мочекислых уратных камней с мягкой структурой. У людей репродуктивного возраста местом локации конкрементов, как правило, являются почки и мочеточник, у пожилых пациентов и детей уролитиаз (мочекаменная болезнь) затрагивает мочевой пузырь. Кроме этого, закисленная микрофлора является благоприятной средой для размножения болезнетворных микроорганизмов.
Наибольшую активность обычно проявляет кишечная палочка (Escherichia coli). Escherichia coli – грамотрицательная бактерия, способная вызвать не только тяжелое отравление. Чрезмерное распространение кишечной палочки может спровоцировать: воспаление мозговых оболочек (менингит), пневмонию, гемолитико-уремический синдром, системное заражение крови (сепсис).
Алкалозу (защелачиванию мочи) соответствуют показатели, превышающие pH 7. В данном случае велика вероятность формирования фосфатов (щелочных конкрементов) в почечных лоханках и чашечках. Особенностью камней фосфатного происхождения является их форсированный рост. При несвоевременной диагностике избавиться от фосфатов можно только хирургическим путем.
Щелочная среда угнетает иммунные функции организма, что способствует проникновению и стремительному развитию бактериальных инфекций мочевого пузыря и почек. Значения pH 8 и выше фиксируются при бактериурии (наличие бактерий в моче). К наиболее опасным инфекциям относятся разновидности Streptococcus (стафилококка):
- Staphylococcus aureus – золотистый стафилококк;
- Staphylococcus epidermidis – эпидермальный стафилококк;
- Staphylococcus saprophyticus – сапрофитный стафилококк.
Колонизация стафилококковых микроорганизмов в моче приводит к развитию бактериального цистита и бактериального пиелонефрита.
Приготовление раствора и калибровка
Мы настоятельно рекомендуем использовать воду, полученную после обратноосмотического фильтра или приобретённую в любом автомагазине дистиллированную воду. Такая вода будет отличается крайне малым содержанием растворённых элементов (ppm). Использование другой воды может значительно повлиять на качество готового раствора и, в дальнейшем, на точность калибровки прибора.
Готовим буферный раствор. Для этого растворяем содержимое пакетиков в 250 мл воды и перемешиваем до полного растворения осадка. PH-метр нужно прополоскать в отдельной ёмкости с чистой водой, чтобы смыть с прибора остатки солей от предыдущих измерений.
Погружаем pH-метр в готовый буферный раствор с кислотностью 4.0
Обратите внимание на показания приборов – эти приборы ранее активно использовались и их показатели далеки от идеальных
Производим калибровку pH-метра. В новой версии прибора, той, что слева, есть функция автоматической калибровки. Для этого нужно удерживать кнопку «Cal» на протяжении 5 секунд. Табло начнёт мигать и предлагать выбрать один из эталонных показателей. Нажатием на эту же кнопку выбираем «4.01». В более старой версии (справа) для калибровки применяется регулировочный винт на обратной стороне, который вращается с помощью небольшой плоской отвёртки. Доводим показатель до эталонного и готовимся к следующему шагу.
Предварительно прополоскав pH-метр в чистой воде, чтобы не смешивать буферные растворы, перемещаем его во вторую ёмкость с буферным раствором 6.86. Производим аналогичные действия что и с раствором 4.00, выбирая нужный показатель на приборе. Затем производим аналогичные действия с раствором 9.18
Готово! Ваш pH-метр откалиброван и готов к работе. Храните прибор в вертикальном положении, налив в колпачок 1-2 мл воды. Измерительная головка электрода прослужит дольше, если не будет полностью пересыхать.
Рекомендуем повторять процедуру калибровки pH-метра один раз в месяц, чтобы быть уверенным в его показаниях.
Способ приготовления
Калибровочный порошок для pH-метра представляет собой смесь в сухом виде. Предварительно ее нужно развести водой. Обязательно использовать дистиллированную, чтобы не изменился pH-баланс. Пропорция: 2 гр. смеси и стакан жидкости (250 мл) с температурой 25 °С
Важно соблюдать указанную дозировку и температурный режим!
Для проведения калибровки опустите измерительный электрод в буферный раствор. На одну процедуру в среднем понадобится 20 мл жидкости. Точность достигает 0,01 единицы. Показатель pH равен 7 и является нейтральным. Форма выпуска — герметично запаянное саше.
Хранение
Держать разведенный порошок для калибровки pH-метра нужно в герметичной таре подальше от солнечных лучей. Желательно избегать долгого хранения в принципе и разводить непосредственно перед процедурой, используя сразу же. В запечатанном пакете сухая субстанция хранится неограниченное количество времени.
Источники
- https://www.gidroponika.su/ph/kalibrovochnye-rastvory.html
- https://interpassazh.ru/aksessuary/vse-dlya-kalibrovki/bufernyye-poroshki-dlya-ph.html
- https://alfaeco.su/shop/ekopribory/poroshki-dlya-kalibrovki-ph-metra/
- https://medtehnika-moskva.ru/poroshok-dlya-kalibrovki-ph-metra.html
- https://www.nv-lab.ru/catalog_info.php?ID=1937&Full=1
- https://www.mirbeer.ru/catalog/pivovarenie/oborudovanie/izmerenie/nabor_dlya_kalibrovki_ph_metra/
Опубликовано: 13.10.2020
рН в организме человека
Различные среды нашего организма также обладают таким показателем:
- кровь – от 7,35 до 7,45;
- слюна – от 6,0 до 7,4;
- пищевод – от 6,0 до 7,0;
- желудочный сок – от 1,0 до 3,5;
- двенадцатиперстная кишка – от 5,6 до 7,9;
- тонкий кишечник – от 7,5 до 8,0;
- толстый кишечник – от 8,5 до 9,0;
- желчь – 7,8.
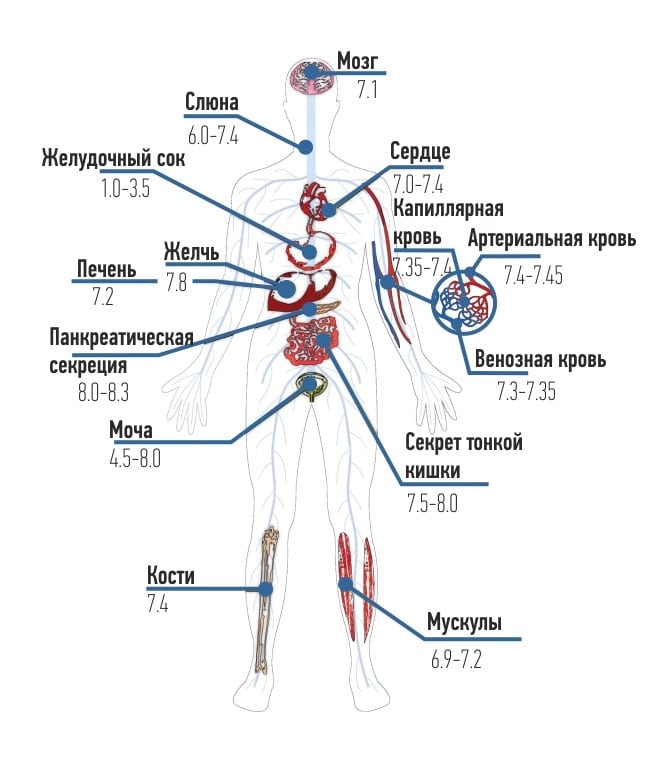
Чтобы наш организм нормально функционировал, необходимо поддерживать адекватный показатель кислотности (так называемое кислотно-щелочное соотношение). Смещение данного соотношения в любую из сторон грозит серьезными заболеваниями, нарушением работы различных органов и систем.
Чаще всего встречается ацидоз – смещение рН в кислую сторону. Он развивается при несбалансированном питании и преобладании в рационе «кислых продуктов» (белый хлеб, газированные напитки и т. д.), при сахарном диабете, злоупотреблении алкоголем. Ацидоз грозит человеку серьезными осложнениями:
- заболевания почек и мочевого пузыря;
- заболевания сердечно-сосудистой системы (включая непосредственно стойкий спазм сосудов, а также уменьшение концентрации кислорода в крови);
- образование камней в мочевыводящей системе;
- общая слабость;
- ожирение;
- появление суставных болей и болевых ощущений в мышцах, связанных с накоплением молочной кислоты;
- сахарный диабет;
- снижение иммунитета;
- увеличение концентрации свободных радикалов в кровотоке, которое может повлечь за собой развитие онкологических заболеваний;
- хрупкость костей.
Кроме того, доказано, что кислая среда – это идеальное условие для развития патогенных микроорганизмов, паразитов, вирусов, поэтому хронический ацидоз может способствовать постоянным воспалительным процессам в организме человека.
Алкалоз или смещение кислотности организма в щелочную сторону – явление редкое, но не менее опасное, чем ацидоз. Оно может встречаться при приеме лекарств, содержащих щелочь, при гипервентиляции легких, неукротимой рвоте, рахите и т. д. Алкалоз может привести к следующим патологиям:
- аллергическим проявлениям, например, кожному зуду;
- заторможенности, апатии;
- нарушению работы сердца;
- потере сознания;
- почечной недостаточности.
- судорожному припадку;
- тошноте, рвоте.
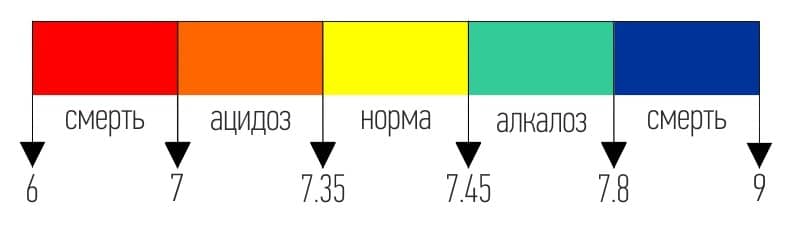
Самым важным является то, что все ферменты нашего организма способны работать только в узком диапазоне рН 7,37 — 7,43, то есть при нормальной рН крови. При сдвиге данного равновесия в любую сторону появляются нарушения тонких механизмов метаболизма и обмена веществ, сбой работы различных органов и систем
Именно поэтому так важно поддерживать этот показатель в пределах нормы
Измерение водородного показателя
Формулы для расчета pH зависят от того, к какому классу относится химическое вещество, входящее в исследуемый раствор, и приведены в специальных справочниках. Более точное значение получают другими методами. Цели и условия проведения исследований определяют, как будет измеряться водородный показатель.
Индикаторные способы
Приблизительно оценить меру активности ионов водорода можно с помощью кислотно-основных индикаторов. Такие вещества обычно относятся к органическим соединениям и имеют свойство изменять свой цвет в разных средах:
- Лакмус меняет цвет от красного в кислой среде через фиолетовый в нейтральной до синего в щелочной.
- Фенолфталеин становится синим в щелочной среде, оставаясь бесцветным в остальных.
- Метилоранж розового цвета соответствует повышенной кислотности, оранжевого — показывает нейтральность среды, в щелочах становится синим.
Изменение происходит для каждого индикатора в своём диапазоне кислотности, обычно составляющем 1—2 единицы. При этом методе результат можно получить быстрый и наглядный при небольших затратах, но недостаточно точный, с большой погрешностью при исследовании очень слабых растворов, окрашенных или мутных вод. Используется, когда нужно найти предварительное определение pH.
Более широкий диапазон и выше точность у универсального индикатора. Он соединяет в себе несколько индикаторов и градуируется в соответствии со значениями pH от единицы до десяти. Соответствие значения водородного показателя и цвета:
- 1 — красный;
- 2 — розовато-оранжевый;
- 3 — оранжевый;
- 4 — темно-желтый;
- 5 — желтый;
- 6 — желтовато-зеленый;
- 7 — светло-зеленый;
- 8 — насыщенный зеленый;
- 9 — сине-зеленый;
- 10 — сине-серый.
Аналитический объемный метод
Кислотно-основное титрирование — метод определения водородного показателя среды с помощью так называемых титрантов. В основном для этого используются сильные кислоты (серная, соляная) и сильные щелочи (едкий калий, каустическая сода).
Раствор-титрант добавляют в исследуемую жидкость по каплям. При этом они вступают в химическую реакцию. Когда она завершается, наступает точка эквивалентности, т. е. момент отчетливого изменения окраски исследуемого раствора. По установленному в результате опыта объему титранта, необходимому для получения точки эквивалентности, и известному значению его концентрации можно рассчитать pH с высокой точностью.
Измерительный прибор pH-метр
Ионометрический метод, при котором кислотный показатель можно измерить с помощью специализированного прибора — pH-метра, является наиболее точным (до сотых от единицы pH), удобным и имеет широкий диапазон измерения. PH-метр представляет собой милливольтметр, способный измерять разность потенциалов со стеклянных электродов. У него также есть система пересчета напряжения в pH.
В исследуемый раствор погружают индикаторный электрод и электрод сравнения, замыкая таким образом гальваническую цепь. Величина электродвижущей силы в ней зависит от активности ионов H+ в растворе, т. е. является функцией только его pH. Индикаторный электрод состоит из стеклянной трубки, заполненной специальной суспензией в растворе соляной кислоты, и погруженной в нее серебряной проволоки.
Специализированный прибор, применяемый в медицине для исследований pH жидкостей желудочно-кишечного тракта, называется ацидогастрометром. Включает в себя регистрирующий блок и один или несколько зондов. Для измерения уровня pH таких биологических жидкостей, как слюна и моча, применяются электронные pH-метры.
Самостоятельное определение pH
Объективно оценить уровень кислотности урины посредством однократного анализа нельзя. При показателях закисления или защелачивания, необходимо провести мониторинг pH. В обязательном порядке самостоятельную оценку показано проводить людям с хроническими патологиями:
- сахарный диабет;
- хронический пиелонефрит;
- дыхательный и респираторный ацидоз;
- хроническая почечная недостаточность;
- метаболический алкалоз;
- почечнокаменная и мочекаменная болезнь.
Регулярно измерять кислотность рекомендуется женщинам в перинатальный период. Существует несколько способов определения значений кислотности в домашних условиях.
Индикаторные тест-полоски
Биосенсор Ури-pH представляет собой одноразовые бумажные стрипы, упакованные в пластиковый тубус. На упаковке размещена специальная тестовая шкала, по которой проводится расшифровка результата. Диапазон шкалы составляет от 5 до 9 единиц. Алгоритм измерения следующий.
Собрать 5–10 мл мочи в стерильную посуду (аптечный контейнер либо предварительно простерилизованную банку), вскрыть тубус и достать стрип с индикатором, погрузить тест в биожидкость на несколько секунд, вынуть стрип и положить на сухую поверхность. Через минуту оценить результат, сравнив оттенок теста и цветовой шкалы на тубусе.
В каждой упаковке экспресс-анализа содержится подробная инструкция
На стрипы для экспресс-анализа нанесен реактив, который при реакции с уриной изменяет цвет. Сравнение цветового оттенка, полученного на стрипе с цветовой шкалой на тубусе, позволяет определить кислотность относительно нормы уровня pH в моче (5–7 единиц). При закислении урины индикатор желтеет или розовеет. Чем светлее цвет, тем выше кислотность урины. Защелачивание изменяет цвет индикатора от сине-зеленого до синего или темно-зеленого.
Справка! Цветовая шкала может иметь несколько вариантов оттенков, близких друг к другу. Эта особенность зависит от производителя тестов.
Анализ методом Магаршака
Это физический метод химического анализа, основанный на изменении окраски специальных растворов. В урину добавляется капля заранее приготовленного индикатора, состоящего из 0,1% спиртового раствора нейтрального красного и метиленового синего раствора аналогичной концентрации. Цвет полученной биожидкости означает уровень pH. Расшифровать цветовой индикатор можно при помощи таблицы:
| Оттенок | Фиолетовый яркий | Фиолетовый светлый | Серый темный | Серо-зеленый | Зеленый |
| ≈ значение | 6,2 | 6,6 | 6,8 | 7,4 | 7,8 |
Лакмусовый индикатор
Лакмусовая бумага – это универсальный индикатор для определения кислой и щелочной среды в любых жидкостях. Основу индикатора составляют природные красящие вещества азолитмин и эритролитмин. Аптечный набор состоит из двух лакмусовых бумажек (индикаторных полосок). Способ использования идентичен тест-полоскам.
В емкость с уриной помещаются обе бумажки, через 30 секунд оценивается полученный результат: если обе полоски остались исходного оттенка, значит, реакция нейтральная, покраснение синей полоски и неизменность цвета красной указывает на закисление, красная полоска стала синей, а синяя осталась неизмененной, означает защелачивание. Недостаток метода заключается в невозможности получить точный цифровой показатель pH. Биосенсор Ури-pH является более информативным способом оценки.
pH-метр портативный
Специальный прибор, предназначенный для оценки кислотного уровня в различных жидкостях. Анализ основан на измерении физических потенциалов в биожидкости, посредством погружения в нее пары электродов. Шкала механического прибора градуирована в рН. Электронная разновидность pH-метра оснащена экраном, на который выводится конкретное цифровое значение.
Существуют лабораторные и портативные приборы. Последний вариант подходит пациентам, вынужденным контролировать pH мочи ежедневно. Перечисленные методики самоконтроля кислотности подходят как для взрослого пациента, так и для ребенка.
Роль pH в химии и биологии.
Кислотность среды имеет важное значение для большинства химических процессов, и возможность протекания либо результат той или иной реакции зачастую зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований либо на производстве применяют буферные растворы, позволяющие сохранять почти постоянное значение pH при разбавлении либо при добавлении в раствор маленьких количеств кислоты либо щёлочи. Водородный показатель pH часто применяют для характеристики кислотно-основных свойств разных биологических сред
Водородный показатель pH часто применяют для характеристики кислотно-основных свойств разных биологических сред.
Для биохимических реакций сильное значение имеет кислотность реакционной среды, протекающих в живых системах
Концентрация в растворе ионов водорода зачастую оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-основного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается под действием буферных систем организма. В человеческом организме в разных органах водородный показатель оказывается разным
В человеческом организме в разных органах водородный показатель оказывается разным.
2.Причины
Возможных причин стойкого повышения кислотности так много, что их обычно делят на две большие группы: эндогенные и экзогенные (внутренние и внешние, соотв.).
К наиболее распространенным эндогенным факторам относятся:
- наследственная предрасположенность;
- хронические инфекции и/или присутствие паразитов;
- стойкая гипоксия (дефицит снабжения тканей и органов кислородом);
- метаболические (обменные) нарушения;
- гиповитаминоз, дефицит микроэлементов, аминокислот и пр.
Основные экзогенные факторы:
- табакокурение и употребление спиртных напитков, в особенности крепких;
- перекосы в ежедневном рационе (увлечение острыми, жирными, пряными, пересоленными, слишком горячими и другими блюдами, раздражающими слизистые оболочки ЖКТ);
- длительный или самодеятельный прием медикаментозных средств без предварительной консультации и контроля гастроэнтеролога;
- работа на некоторых вредных производствах, подразумевающих, в частности, постоянный контакт с нитратами;
- гиподинамия, сидячий образ жизни, бессистемное питание с длительными перерывами и преобладанием бутербродов, фастфуда, кислых соков, кофе, газированных напитков и тому подобных «убийц желудка».
Показания
Назначение и расшифровку ОАМ проводят специалисты: нефролог, гинеколог, инфекционист, уролог, педиатр, терапевт и др.
- Плановое профилактическое обследование, диспансеризация;
- Обязательное исследование при постанове на учет по беременности, регулярный контроль при ведении беременности;
- Подозрение на заболевания органов мочеполовой системы (пиелонефрит, гломерулонефрит, пиелит, цистит, уретрит, почечная недостаточность и др.);
- Диагностированные патологии почек, мочевыводящих каналов, мочевого пузыря (контроль течения заболевания и эффективности применяемого лечения);
- Мониторинг состояния здоровья пациентов с повышенной кислотностью желудочного секрета;
- Обязательный контроль эффективности водной терапии при лечении минеральными водами;
- Ацидоз или алкалоз различной этиологии;
- Гематурия (примесь крови в моче);
- Диарея и/или рвота в течение длительного времени (риск развития обезвоживания);
- Сахарный диабет (риск развития хронического ацидоза);
- Лихорадочные состояния, сопровождающиеся повышением температуры тела и обильным потоотделением;
- Реабилитационный период после голодания, соблюдения постов, строгих диет;
- Гипокалиемия (дефицит калия в организме) и гипохлоремия (недостаток хлора);
- Контроль состояния пациента после внутривенного вливания значительных объемов изотонического раствора натрия хлорида;
- Экссудативный диатез у детей (аллергическое поражение слизистой и кожи).
Набор для калибровки Ph-метра
Набор состоит из 2-х пакетов с калибровочными порошками, каждый из которых имеет свой уровень pH. Имея такой комплект, появляется возможность калибровать практически любой портативный pH метр, следить за точностью его показаний и получать заведомо достоверные данные.Раствор pH 4.01Раствор pH 6.86Срок годности фиксанала в закрытом состоянии: неограничен.Хранить в сухом, защищённом от света месте, при комнатной температуре. Проверяйте точность Вашего pH-метра согласно прилагаемой к нему инструкции.Приготовление буферного раствора для калибровки:
Для приготовления калибровочного (буферного) раствора берется пластиковый или стеклянный сосуд 250 мл с видимыми делениями объема. В сосуд высыпается фиксанал и через воронку аккуратно наливается дистиллированная, или деионизованная вода (с температурой равной 25⁰С), объем доводится до 250 мл и размешивается. Калибровочный раствор готов.Величина pH для калибровочного раствора зависит от температуры. Эта зависимость указана в таблице на обороте пакета с фиксаналом. Для точной калибровки электродов с использованием буферных растворов необходимо измерять температуру, при которой используется раствор
После этого прибор должен быть прокалиброван по соответствующему значению pH.Важно! Буферные растворы портятся при воздействии на них воздуха и света. Поэтому их следует хранить в герметичных непрозрачных емкостях, при комнатной температуре, в защищённом от света месте.Калибровка pH-метра:Погрузите pH-метр в раствор, имеющий температуру 25⁰С, слегка помешивая в течение примерно 30 сек
Подождите пока показания на экране/дисплее прибора стабилизируются. Как правило, калибровка производится вращением подстроечного винта. Значения, которые показывает прибор, должны совпадать с известным значением pH калибровочного раствора.Буферные порошки смешивают с дистиллированной водой для приготовления свежего калибровочного раствора для калибровки pH-метра в нужное время.Многие рН метры имеют заводскую калибровку и готовы к использованию сразу после покупки. Возможно, что заводской калибровки будет недостаточно для ваших нужд, поэтому все рН-метры должны быть откалиброваны пользователем. Например, если тестирование будет проводиться в кислотных растворах, то рН-метр должен быть откалиброван значением рН 4,1 для достижения более точных результатов. РH метр может быть откалиброван по одной, двум или трем точкам. Производители чаще всего рекомендуют, по крайней мере, две точки для калибровки для оптимального тестирования. Как часто калибровать pH-метр ?
- Если вы предполагаете, что показания некорректны
- Если тестируются агрессивные жидкости (очень кислотные или очень щелочные)
- После замены электрода

















